목차
○ 공동 실험자 학과, 학번, 이름
○ 실험 날짜
○ 실험 방법
○ 실험 결과
① 백열등
② 수소 (hydrogen)
③ 수은 (mercury)
③ 나트륨 (Sodium)
○ 결과 분석
○ 토의 및 토론
○ 실험 날짜
○ 실험 방법
○ 실험 결과
① 백열등
② 수소 (hydrogen)
③ 수은 (mercury)
③ 나트륨 (Sodium)
○ 결과 분석
○ 토의 및 토론
본문내용
nm)>
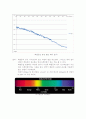
결과 : 수소를 실험 할 때 전류를 흘러 줬을 때 수소의 색깔을 알고 있었기 때문에 쉽게 수소라는 것을 예측할 수 있었고 이미 알려진 수소의 선스펙트럼이 나 타나는 파장을 이용하여 그 주위에서의 파장을 0.05nm의 단위로 측정하여 수소의 선스펙트럼을 찾을 수 있었다.
우리의 실험에서 첫 번째 선은 파장이 410.25nm에서 전압이 -0.491V가 나왔으며 두 번째 선은 파장이 434nm에서 전압이 -0.521V가 나왔다. 세 번째 선은 파장이 485.7nm에서 전압이 -0.578V가 나왔고 마지막 네 번째 선은 파장이 656.2nm에서 전압이 -1.903V가 나왔다. 이 값은 아래와 같이 이미 알려진 수소의 선스펙트럼과 거의 일치한다.
<수소 선스펙트럼>
③ 수은 (mercury)
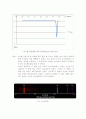
<수은>
<수은을 분광했을 때의 결과>
결과 : 이번 실험에서 수은 역시 미리 수은을 따로 준비하였기 때문에 이미 알려진 수소의 선스펙트럼의 결과를 가지고 선스펙트럼이 측정되는 파장 주위에서 0.05nm단위로 측정하였다. 이번 실험에서 파장이 365nm 일 때 전압이 -0.531V로 첫 번째 선이 나타났으며 404.7nm에서 전압-0.505V로 두 번 째 선이, 435.9nm에서 전압 -0.544V로 세 번째 선이 나타나고 네 번째 선은 546.1nm에서 전압-0.544V가 나왔다. 수은의 경우 아래와 같이 이미 알려진 바에 따르면 총 5개의 선이 더 나와야 하는데 계속적인 반복실험에 도 600nm이상에서는 오실로스코프의 떨림이 관측되지 않아 측정 할 수가 없었다. 또한 404.7nm와 407.8nm에서 따로 두 개의 선이 나타나야 하지만 우리 실험에서는 구분 없이 한 구간처럼 나타났다.
<수은의 선스펙트럼>
③ 나트륨 (Sodium)
<나트륨>
<나트륨을 분광했을 때의 결과>
결과 : 이번 실험은 실험목적에 맞게 실험관 안에 들어있는 원자에 대한 아무런 정보 없이 시작하였다. 임의로 하나를 선택하여 전류를 흘러주고 넓은 범위 (200nm~600nm)로 파장을 변화시켰을 때 오실로 스코프의 떨림을 보았 다. 이 때 범위 내에서 오실로 스코프가 마지막에 두 번 떨림을 관찰하였고 이미 알려져 있는 여러 가지 원소에 대한 스펙트럼을 분석하여 놓은 것을 비교하여 나트륨이 두 번 떨리는 것을 보았다. 이것으로 1차적으로 나트 륨이라는 예상을 할 수 있었고 나트륨의 선스펙트럼이 나타나는 구간을 측 정하였을 때 나트륨의 선스펙트럼이 나타남을 볼 수 있었고 이것으로 실험 관 안에 들어있는 원자가 나트륨임을 알 수 있었다. 실험에서 파장이 585nm에서 전압 -0.668V로 첫 번째 선이 나타났으며 파장 594.5nm에서 전압 -0.677V로 두 번째 선이 나타났다.
<나트륨의 선스펙트럼>
○ 결과 분석
수소의 경우 선스펙트럼이 발견되는 구간의 Pick Point에서의 파장은 410.25nm, 434nm, 485.7nm, 656.2nm이 나왔다.
이것을 발머공식
을 통해 얻은 수소 선스펙트럼의 파장은 410.1nm, 433.9nm, 486.0nm, 656.1nm이다.
오차를 구하면
을 이용하여 구한다.
구간 Ⅰ:
구간 Ⅱ :
구간 Ⅲ :
구간 Ⅳ :
오차범위 0.06%내의 거의 정확한 값을 얻었다.
이제 수소이온화 에너지를 구한다.
이때 수소원자는 양전하를 가진 무거운 핵과 그 주위를 원운동하는 전자 1개로 구성이 되어있고 전자는 (n=1,2,3...)의 궤도조건을 만족한다. 이렇게 되면 고전이론과 달리 전자는 에너지를 잃지 않는다.
이때 전자가 다른 궤도로 전이할 때는 을 따라 에너지를 방출하거나 흡수한다.
이제 보어의 수소원자 모형을 보면 핵과 전자간의 인력과 전자의 원심력이 같아야 하므로 을 만족해야하고 여기에 조건을 대입하여 r을 구하면 이 된다. 여기에 전자의 m, e, h값은 이미 알려진 값이므로 대입을 하면
을 얻을 수 있다.
이제 에너지를 계산 할 때 임의상태의 전체 에너지는 운동에너지와 Potential 에너지의 합이라는 사실을 이용하여 이 된다. 여기에 위에서 구한 r값을 대입하면 가 된다. 궤도들의 에너지를 그림으로 나타내면 다음과 같다.
<에너지 준위>
이때 n=1일 때 에너지가 가장 낮은데 이때를 수소의 바닥상태라고 한다.
즉 , 가 되고 일 때 에너지 차이는 가 되고 이것이 수소의 이온화 에너지이다.
○ 토의 및 토론
우선 이번 실험에서 전반적으로 분광기를 통해 측정한 값을 그래프로 나타내었을 때 선이 날카롭지 못하고 약간 퍼진 모습을 가진다. 이것은 실험을 할 때 측정이 잘 되게 하기 위하여 분광기의 슬릿을 열어놓았기 때문에 그래프가 둥글게 나왔다. 만약 슬릿의 간격을 좁혔다면 그래프의 모양이 더욱 날카로웠을 것이다.
그리고 수소를 측정하였을 경우 이미 알려진 값과 거의 일치하게 나왔는데 이것은 계통오차가 거의 없다는 것이다. 즉, 파장의 구간을 측정하는 것은 사람이 하는 것이 아니라 기계가 하기 때문에 오차가 작다.
이번 실험에서 가장 잘못된 점은 수은을 측정하는 과정에 있어서 파장이 600nm 이상 일 때 오실로 스코프의 떨림이 전혀 없어서 더 이상 측정을 하지 못하였다. 실험하기 전 수은을 분광하는 것을 알았기 때문에 이미 알려진 수은의 파장을 보고 600nm이상일 때 나타나야하는 것을 알았기 때문에 반복적으로 실험을 하였지만 측정이 되지 않아 600nm이하의 파장에서만 측정을 하였다.
마지막 나트륨의 경우 200-600nm사이에서 마지막에 오실로스코프의 떨림이 두 번 일어나는 것을 보고 나트륨인 것을 예상할 수 있었다. 하지만 나트륨의 경우 파장사이의 간격이 좁아 분광기의 슬릿을 많이 열어 논 상태였기 때문에 깔끔한 모양의 그래프를 얻는 분광에는 실패하였다.
이번 실험에서 슬릿의 열어 논 상태와 다른 분광기로 다른 빛이 들어가지 않도록 하는 실험은 계통오차로써 충분히 예상 할 수 있었고 조금 더 계통오차를 줄였다면 더욱 정확한 실험을 할 수 있었을 것이다. 이것 외에 전압을 측정하는 것 역시 컴퓨터에 출력되는 변화되는 출력 값을 가지고 그래프를 만들기 때문에 이 과정에서도 더욱 많은 데이터로 평균을 구했으면 오차를 줄일 수 있었을 것이다.
결과 : 수소를 실험 할 때 전류를 흘러 줬을 때 수소의 색깔을 알고 있었기 때문에 쉽게 수소라는 것을 예측할 수 있었고 이미 알려진 수소의 선스펙트럼이 나 타나는 파장을 이용하여 그 주위에서의 파장을 0.05nm의 단위로 측정하여 수소의 선스펙트럼을 찾을 수 있었다.
우리의 실험에서 첫 번째 선은 파장이 410.25nm에서 전압이 -0.491V가 나왔으며 두 번째 선은 파장이 434nm에서 전압이 -0.521V가 나왔다. 세 번째 선은 파장이 485.7nm에서 전압이 -0.578V가 나왔고 마지막 네 번째 선은 파장이 656.2nm에서 전압이 -1.903V가 나왔다. 이 값은 아래와 같이 이미 알려진 수소의 선스펙트럼과 거의 일치한다.
<수소 선스펙트럼>
③ 수은 (mercury)
<수은>
<수은을 분광했을 때의 결과>
결과 : 이번 실험에서 수은 역시 미리 수은을 따로 준비하였기 때문에 이미 알려진 수소의 선스펙트럼의 결과를 가지고 선스펙트럼이 측정되는 파장 주위에서 0.05nm단위로 측정하였다. 이번 실험에서 파장이 365nm 일 때 전압이 -0.531V로 첫 번째 선이 나타났으며 404.7nm에서 전압-0.505V로 두 번 째 선이, 435.9nm에서 전압 -0.544V로 세 번째 선이 나타나고 네 번째 선은 546.1nm에서 전압-0.544V가 나왔다. 수은의 경우 아래와 같이 이미 알려진 바에 따르면 총 5개의 선이 더 나와야 하는데 계속적인 반복실험에 도 600nm이상에서는 오실로스코프의 떨림이 관측되지 않아 측정 할 수가 없었다. 또한 404.7nm와 407.8nm에서 따로 두 개의 선이 나타나야 하지만 우리 실험에서는 구분 없이 한 구간처럼 나타났다.
<수은의 선스펙트럼>
③ 나트륨 (Sodium)
<나트륨>
<나트륨을 분광했을 때의 결과>
결과 : 이번 실험은 실험목적에 맞게 실험관 안에 들어있는 원자에 대한 아무런 정보 없이 시작하였다. 임의로 하나를 선택하여 전류를 흘러주고 넓은 범위 (200nm~600nm)로 파장을 변화시켰을 때 오실로 스코프의 떨림을 보았 다. 이 때 범위 내에서 오실로 스코프가 마지막에 두 번 떨림을 관찰하였고 이미 알려져 있는 여러 가지 원소에 대한 스펙트럼을 분석하여 놓은 것을 비교하여 나트륨이 두 번 떨리는 것을 보았다. 이것으로 1차적으로 나트 륨이라는 예상을 할 수 있었고 나트륨의 선스펙트럼이 나타나는 구간을 측 정하였을 때 나트륨의 선스펙트럼이 나타남을 볼 수 있었고 이것으로 실험 관 안에 들어있는 원자가 나트륨임을 알 수 있었다. 실험에서 파장이 585nm에서 전압 -0.668V로 첫 번째 선이 나타났으며 파장 594.5nm에서 전압 -0.677V로 두 번째 선이 나타났다.
<나트륨의 선스펙트럼>
○ 결과 분석
수소의 경우 선스펙트럼이 발견되는 구간의 Pick Point에서의 파장은 410.25nm, 434nm, 485.7nm, 656.2nm이 나왔다.
이것을 발머공식
을 통해 얻은 수소 선스펙트럼의 파장은 410.1nm, 433.9nm, 486.0nm, 656.1nm이다.
오차를 구하면
을 이용하여 구한다.
구간 Ⅰ:
구간 Ⅱ :
구간 Ⅲ :
구간 Ⅳ :
오차범위 0.06%내의 거의 정확한 값을 얻었다.
이제 수소이온화 에너지를 구한다.
이때 수소원자는 양전하를 가진 무거운 핵과 그 주위를 원운동하는 전자 1개로 구성이 되어있고 전자는 (n=1,2,3...)의 궤도조건을 만족한다. 이렇게 되면 고전이론과 달리 전자는 에너지를 잃지 않는다.
이때 전자가 다른 궤도로 전이할 때는 을 따라 에너지를 방출하거나 흡수한다.
이제 보어의 수소원자 모형을 보면 핵과 전자간의 인력과 전자의 원심력이 같아야 하므로 을 만족해야하고 여기에 조건을 대입하여 r을 구하면 이 된다. 여기에 전자의 m, e, h값은 이미 알려진 값이므로 대입을 하면
을 얻을 수 있다.
이제 에너지를 계산 할 때 임의상태의 전체 에너지는 운동에너지와 Potential 에너지의 합이라는 사실을 이용하여 이 된다. 여기에 위에서 구한 r값을 대입하면 가 된다. 궤도들의 에너지를 그림으로 나타내면 다음과 같다.
<에너지 준위>
이때 n=1일 때 에너지가 가장 낮은데 이때를 수소의 바닥상태라고 한다.
즉 , 가 되고 일 때 에너지 차이는 가 되고 이것이 수소의 이온화 에너지이다.
○ 토의 및 토론
우선 이번 실험에서 전반적으로 분광기를 통해 측정한 값을 그래프로 나타내었을 때 선이 날카롭지 못하고 약간 퍼진 모습을 가진다. 이것은 실험을 할 때 측정이 잘 되게 하기 위하여 분광기의 슬릿을 열어놓았기 때문에 그래프가 둥글게 나왔다. 만약 슬릿의 간격을 좁혔다면 그래프의 모양이 더욱 날카로웠을 것이다.
그리고 수소를 측정하였을 경우 이미 알려진 값과 거의 일치하게 나왔는데 이것은 계통오차가 거의 없다는 것이다. 즉, 파장의 구간을 측정하는 것은 사람이 하는 것이 아니라 기계가 하기 때문에 오차가 작다.
이번 실험에서 가장 잘못된 점은 수은을 측정하는 과정에 있어서 파장이 600nm 이상 일 때 오실로 스코프의 떨림이 전혀 없어서 더 이상 측정을 하지 못하였다. 실험하기 전 수은을 분광하는 것을 알았기 때문에 이미 알려진 수은의 파장을 보고 600nm이상일 때 나타나야하는 것을 알았기 때문에 반복적으로 실험을 하였지만 측정이 되지 않아 600nm이하의 파장에서만 측정을 하였다.
마지막 나트륨의 경우 200-600nm사이에서 마지막에 오실로스코프의 떨림이 두 번 일어나는 것을 보고 나트륨인 것을 예상할 수 있었다. 하지만 나트륨의 경우 파장사이의 간격이 좁아 분광기의 슬릿을 많이 열어 논 상태였기 때문에 깔끔한 모양의 그래프를 얻는 분광에는 실패하였다.
이번 실험에서 슬릿의 열어 논 상태와 다른 분광기로 다른 빛이 들어가지 않도록 하는 실험은 계통오차로써 충분히 예상 할 수 있었고 조금 더 계통오차를 줄였다면 더욱 정확한 실험을 할 수 있었을 것이다. 이것 외에 전압을 측정하는 것 역시 컴퓨터에 출력되는 변화되는 출력 값을 가지고 그래프를 만들기 때문에 이 과정에서도 더욱 많은 데이터로 평균을 구했으면 오차를 줄일 수 있었을 것이다.






























소개글