본문내용
의 증발을 방해하기 때문이다.
다시 말해 소금물의 소금이 물 분자를 끓어 당기고 물 분자 끼리 또 끓어 당겨 [수소 결합을 한 분자 -- 분산력, 이중 극자 사이의 힘, 수소 결합] 소금과의 상호 작용 힘을 플러스 시킨 것 이다.
2> 녹는점이 다른 이유
녹는점이란 용융점 또는 융해점이라고도 한다. 녹는 물질이 순수한 물질이라면 그 물질이 녹는 동안 가열하여도 온도가 일정하게 유지되는 일정 온도구간이 나타나며 고체와 액체가 공존할 때의 온도를 녹는점이라 한다. 순수한 물질은 녹는점과 어는점(freezing point)이 항상 같으며 각 물질마다 녹는점은 모두 다르므로 그 물질만이 가지는 고유한 성질인 물질의 특성이 된다. 예를 들어 얼음은 0℃에서 녹고, 물은 같은 온도 0℃에서 언다.
가열곡선(heating curve)에서 보이는 녹는점에서 일정온도 구간이 나타나는 이유는 고체가 녹고 있는 동안 흡수한 열이 물질의 상태를 고체 상태에서 액체 상태로 변화시키는 데에 모두 쓰이기 때문이다. 일반적으로 압력 1기압(1atm)에서의 융해온도를 그 물질의 녹는점이라 하며 불순물이 함유되어 있거나 압력이 변하면 녹는점도 달라진다. 유리, 플라스틱 등 비결정질(非結晶質)고체에는 녹는점이 뚜렷하게 나타나지 않는다.
녹는점이 이렇다면 녹는점이 물질마다 다른 이유는 바로 분자간에 작용하는 인력이 다르기 때문이다.
분자간의 인력은 분자의 질량에 달려있다. 질량으로 인한 만유인력이 인력이기 때문이다. 그러므로 물질마다 분자량이 다르기 때문 녹는점이 다른 것이다. 이는 수소, 산소와 같은 물질에서만 이다. 이는 분자 구조상 대칭을 이루어 전기적 성질을 띄지 않기 때문에 만유인력만 작용한다.
그러나 물이나 이산화탄소같이 비대칭을 이루어 전기적 성질을 띌 경우 인력에는 만유인력 외에도 전기력이 작용하기 때문에 더욱더 떼어내기가 어렵다다. 즉, 물 분자 내에서도 +극과 -극이 생겨 분자끼리 자석처럼 끌어당긴다는 것이다. 그것이 밀도가 비슷한 다른 물질들 보다 물이 녹는점이 높은 이유이다. 전기력이 더욱더 분자들을 강하게 속박하기 때문입니다.
2) 온도계를 보정해야 하는 이유는 무엇인가?
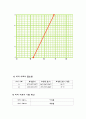
여러 제조사에서 만든 온도계로 특정 시료의 온도를 측정하면 온도계마다 약간의 차이가 나타나며 문헌 값과도 조금씩 차이가 나므로 정확한 온도를 측정하기가 쉽지 않다. 따라서 정확한 측정값을 얻기 위해서는 온도계를 보정해 주어야 한다. 여러 가지 표준물질의 녹는점을 측정하여 측정된 온도와 문헌 값과의 차이를 가지고 온도 보정 그래프로 그리고 이를 바탕으로 새롭게 측정하는 온도를 보정해 주면 된다.
3) 녹는점, 끓는점에서 온도가 유지되는 이유는?
고체상태의 물(얼음)은 액체상태의 물보다 결합력이 강하다. 그러므로 결합을 끊고 액체 상태로 만드려면 에너지가 필요하다. 가해주는 열(에너지)는 물의 온도를 올리는 대신 결합을 끊는데 사용되고 당연히 결합을 끊는동안 물의 온도는 올라가지 않는다. 이때의 온도를 녹는점(melting point)이라 한다.
마찬가지로 액체상태의 물은 기체상태의 물(수증기)보다 결합력이 강하므로 결합을 끊고 기체상태로 만들기 위해 에너지가 필요하며 같은 이유로 에너지가 분자사이의 결합을 끊는데 사용되므로 온도는 올라가지 않고 일정하게 유지된다. 이때의 온도를 끓는점(boiling point)라 한다.
4) 녹는점과 끓는점을 측정하는 기기를 찾아보고 간단히 설명하라.
온도계
물체나 어떠한 공간에서의 온도를 측정하는 기구로 화씨온도계는 파렌하이트가 1714년에, 섭씨온도계는 1742년에 셀시우스가 만들었다.
온도계를 만든 것은 과학의 발달사에서 가장 획기적인 사건 중의 하나이다. 열을 측정하고자 하는 노력이 온도계 제작에 대한 열의로 이어지면서, 17세기 초 이미 갈릴레이와 그의 제자들은 온도를 측정하는 문제를 생각하기 시작하였고 기체온도계를 만들게 되었다. 그러나 정확한 온도측정이 가능한 것은 액체 온도계인 알코올, 수은온도계가 만들어진 이후부터이며 온도변화에 따른 부피팽창과 수축이 큰 알코올온도계, 수은온도계의 제작으로 18세기 이후 열에 대한 연구는 획기적인 발전을 이루게 되었다.
온도계의 역사
1714년 파렌하이트(Fahrenheit)는 수은을 이용한 온도계로 물의 어는점(32℉)과 끓는점(212℉) 사이를 180 등분한 화씨온도계를 만들었으며, 1742년 셀시우스(Celicus)는 물의 어는점(0℃)과 끓는점(100℃) 사이를 100 등분한 온도계를 제작하여 전세계 사람들이 오늘날 공통적으로 사용하는 섭씨온도계를 만들어 내었다.
온도의 척도
온도의 척도에는 화씨온도, 섭씨온도가 있다. 화씨온도는 주로 미국에서 사용하며 대부분의 나라에서나 과학분야에서는 섭씨온도를 사용한다. SI단위계에서는 온도의 척도로 켈빈온도(절대온도)를 사용하며 켈빈온도척도에서 0도는 이론적으로 가능한 최저온도로 이 온도에서 열에너지는 0이 된다.
알코올온도계와 수은온도계
주위의 온도변화에 따른 부피팽창률과 수축률이 큰 액체온도계로 유리관과 온도계의 구부로 구성되어 있다. 저온온도계인 알코올온도계의 구부에 담겨진 빨간색은 알코올의 무색에 눈에 띄기 쉽도록 빨간색으로 착색한 것으로 가열되어 온도가 올라감에 따라 유리관에 빨간 기둥이 나타나면서 온도측정이 가능하게 된다.빨간 기둥의 가운데 움푹 패인 부분을 일직선으로 하여 읽어주면 그때의 온도가 된다. 고온온도계인 수은온도계는 알코올 온도계보다 온도변화에 따른 부피팽창이 일정하여 일반적으로 더 정확한 온도측정에는 수은온도계가 사용된다. 눈금을 읽을 때는 온도계의 기둥 높이와 눈의 높이를 같게 하고 온도계와 30㎝정도 떨어져서 읽는다.
6. Discussion (토의 및 고찰)
이번 실험을 통해서 표준물질의 녹는점을 이용하여 측정된 온도와 문헌 값과의 차이를 가지고 온도보정 그래프로 온도를 보정하는 방법을 알게 되었고, 그 값을 통하여 미지의 시료의 끓는점을 측정하여 보정된 온도계로 문헌 값과의 비교를 통하여 미지 시료가 어떤 화합물인지 알아내는 방법을 알게 되었다.
7. References (참고문헌)
naver, google, 재미있는 일반화학 실험
다시 말해 소금물의 소금이 물 분자를 끓어 당기고 물 분자 끼리 또 끓어 당겨 [수소 결합을 한 분자 -- 분산력, 이중 극자 사이의 힘, 수소 결합] 소금과의 상호 작용 힘을 플러스 시킨 것 이다.
2> 녹는점이 다른 이유
녹는점이란 용융점 또는 융해점이라고도 한다. 녹는 물질이 순수한 물질이라면 그 물질이 녹는 동안 가열하여도 온도가 일정하게 유지되는 일정 온도구간이 나타나며 고체와 액체가 공존할 때의 온도를 녹는점이라 한다. 순수한 물질은 녹는점과 어는점(freezing point)이 항상 같으며 각 물질마다 녹는점은 모두 다르므로 그 물질만이 가지는 고유한 성질인 물질의 특성이 된다. 예를 들어 얼음은 0℃에서 녹고, 물은 같은 온도 0℃에서 언다.
가열곡선(heating curve)에서 보이는 녹는점에서 일정온도 구간이 나타나는 이유는 고체가 녹고 있는 동안 흡수한 열이 물질의 상태를 고체 상태에서 액체 상태로 변화시키는 데에 모두 쓰이기 때문이다. 일반적으로 압력 1기압(1atm)에서의 융해온도를 그 물질의 녹는점이라 하며 불순물이 함유되어 있거나 압력이 변하면 녹는점도 달라진다. 유리, 플라스틱 등 비결정질(非結晶質)고체에는 녹는점이 뚜렷하게 나타나지 않는다.
녹는점이 이렇다면 녹는점이 물질마다 다른 이유는 바로 분자간에 작용하는 인력이 다르기 때문이다.
분자간의 인력은 분자의 질량에 달려있다. 질량으로 인한 만유인력이 인력이기 때문이다. 그러므로 물질마다 분자량이 다르기 때문 녹는점이 다른 것이다. 이는 수소, 산소와 같은 물질에서만 이다. 이는 분자 구조상 대칭을 이루어 전기적 성질을 띄지 않기 때문에 만유인력만 작용한다.
그러나 물이나 이산화탄소같이 비대칭을 이루어 전기적 성질을 띌 경우 인력에는 만유인력 외에도 전기력이 작용하기 때문에 더욱더 떼어내기가 어렵다다. 즉, 물 분자 내에서도 +극과 -극이 생겨 분자끼리 자석처럼 끌어당긴다는 것이다. 그것이 밀도가 비슷한 다른 물질들 보다 물이 녹는점이 높은 이유이다. 전기력이 더욱더 분자들을 강하게 속박하기 때문입니다.
2) 온도계를 보정해야 하는 이유는 무엇인가?
여러 제조사에서 만든 온도계로 특정 시료의 온도를 측정하면 온도계마다 약간의 차이가 나타나며 문헌 값과도 조금씩 차이가 나므로 정확한 온도를 측정하기가 쉽지 않다. 따라서 정확한 측정값을 얻기 위해서는 온도계를 보정해 주어야 한다. 여러 가지 표준물질의 녹는점을 측정하여 측정된 온도와 문헌 값과의 차이를 가지고 온도 보정 그래프로 그리고 이를 바탕으로 새롭게 측정하는 온도를 보정해 주면 된다.
3) 녹는점, 끓는점에서 온도가 유지되는 이유는?
고체상태의 물(얼음)은 액체상태의 물보다 결합력이 강하다. 그러므로 결합을 끊고 액체 상태로 만드려면 에너지가 필요하다. 가해주는 열(에너지)는 물의 온도를 올리는 대신 결합을 끊는데 사용되고 당연히 결합을 끊는동안 물의 온도는 올라가지 않는다. 이때의 온도를 녹는점(melting point)이라 한다.
마찬가지로 액체상태의 물은 기체상태의 물(수증기)보다 결합력이 강하므로 결합을 끊고 기체상태로 만들기 위해 에너지가 필요하며 같은 이유로 에너지가 분자사이의 결합을 끊는데 사용되므로 온도는 올라가지 않고 일정하게 유지된다. 이때의 온도를 끓는점(boiling point)라 한다.
4) 녹는점과 끓는점을 측정하는 기기를 찾아보고 간단히 설명하라.
온도계
물체나 어떠한 공간에서의 온도를 측정하는 기구로 화씨온도계는 파렌하이트가 1714년에, 섭씨온도계는 1742년에 셀시우스가 만들었다.
온도계를 만든 것은 과학의 발달사에서 가장 획기적인 사건 중의 하나이다. 열을 측정하고자 하는 노력이 온도계 제작에 대한 열의로 이어지면서, 17세기 초 이미 갈릴레이와 그의 제자들은 온도를 측정하는 문제를 생각하기 시작하였고 기체온도계를 만들게 되었다. 그러나 정확한 온도측정이 가능한 것은 액체 온도계인 알코올, 수은온도계가 만들어진 이후부터이며 온도변화에 따른 부피팽창과 수축이 큰 알코올온도계, 수은온도계의 제작으로 18세기 이후 열에 대한 연구는 획기적인 발전을 이루게 되었다.
온도계의 역사
1714년 파렌하이트(Fahrenheit)는 수은을 이용한 온도계로 물의 어는점(32℉)과 끓는점(212℉) 사이를 180 등분한 화씨온도계를 만들었으며, 1742년 셀시우스(Celicus)는 물의 어는점(0℃)과 끓는점(100℃) 사이를 100 등분한 온도계를 제작하여 전세계 사람들이 오늘날 공통적으로 사용하는 섭씨온도계를 만들어 내었다.
온도의 척도
온도의 척도에는 화씨온도, 섭씨온도가 있다. 화씨온도는 주로 미국에서 사용하며 대부분의 나라에서나 과학분야에서는 섭씨온도를 사용한다. SI단위계에서는 온도의 척도로 켈빈온도(절대온도)를 사용하며 켈빈온도척도에서 0도는 이론적으로 가능한 최저온도로 이 온도에서 열에너지는 0이 된다.
알코올온도계와 수은온도계
주위의 온도변화에 따른 부피팽창률과 수축률이 큰 액체온도계로 유리관과 온도계의 구부로 구성되어 있다. 저온온도계인 알코올온도계의 구부에 담겨진 빨간색은 알코올의 무색에 눈에 띄기 쉽도록 빨간색으로 착색한 것으로 가열되어 온도가 올라감에 따라 유리관에 빨간 기둥이 나타나면서 온도측정이 가능하게 된다.빨간 기둥의 가운데 움푹 패인 부분을 일직선으로 하여 읽어주면 그때의 온도가 된다. 고온온도계인 수은온도계는 알코올 온도계보다 온도변화에 따른 부피팽창이 일정하여 일반적으로 더 정확한 온도측정에는 수은온도계가 사용된다. 눈금을 읽을 때는 온도계의 기둥 높이와 눈의 높이를 같게 하고 온도계와 30㎝정도 떨어져서 읽는다.
6. Discussion (토의 및 고찰)
이번 실험을 통해서 표준물질의 녹는점을 이용하여 측정된 온도와 문헌 값과의 차이를 가지고 온도보정 그래프로 온도를 보정하는 방법을 알게 되었고, 그 값을 통하여 미지의 시료의 끓는점을 측정하여 보정된 온도계로 문헌 값과의 비교를 통하여 미지 시료가 어떤 화합물인지 알아내는 방법을 알게 되었다.
7. References (참고문헌)
naver, google, 재미있는 일반화학 실험
키워드
추천자료
 VOC[휘발성유기화합물]
VOC[휘발성유기화합물] 방향족 니트로 화합물의 합성 및 확인보고서
방향족 니트로 화합물의 합성 및 확인보고서 맥스웰방정식의 물리적의미및 유도과정
맥스웰방정식의 물리적의미및 유도과정 알데히드화합물(화학)
알데히드화합물(화학) 부모의 양육기술부족으로 인한 물리적 방임사례
부모의 양육기술부족으로 인한 물리적 방임사례 수질관리 (물리적 화학적 생물학적 처리방법)
수질관리 (물리적 화학적 생물학적 처리방법) 유지의 이화학적 성질 (물리적, 화학적)
유지의 이화학적 성질 (물리적, 화학적) [생활속 탄소 화합물] 아스피린, 아세트아미노펜, 이부프로펜, 비타민C등에 대해서
[생활속 탄소 화합물] 아스피린, 아세트아미노펜, 이부프로펜, 비타민C등에 대해서 유기화학실험 - 유기화합물의 재결정
유기화학실험 - 유기화합물의 재결정 [유기화학실험] 유기화합물의 용해도
[유기화학실험] 유기화합물의 용해도 [화학공학실험] 기기분석 - GC(가스크로마토그래피)를 이용하여 휘발성 유기화합물 정량분석
[화학공학실험] 기기분석 - GC(가스크로마토그래피)를 이용하여 휘발성 유기화합물 정량분석 알케인의 물리적 성질 & 알켄의 화학적 성질.pptx
알케인의 물리적 성질 & 알켄의 화학적 성질.pptx e-비즈니스)인터넷의 다양한 주소(Address) 체계에 대해 기술. 이 경우에 물리적 주소와 논리...
e-비즈니스)인터넷의 다양한 주소(Address) 체계에 대해 기술. 이 경우에 물리적 주소와 논리... 인터넷의 다양한 주소(Address) 체계에 대해 기술. 이 경우에 물리적 주소와 논리적 주소 등...
인터넷의 다양한 주소(Address) 체계에 대해 기술. 이 경우에 물리적 주소와 논리적 주소 등...






























소개글